Порошок йодату калію для харчового реагенту медичного класу
Опис продукту
Назва продукту: Йодат калію
Чистота: 99,5%;
CAS:7758-05-6
МФ: IKO3
МВт: 214
EINECS: 231-831-9
Температура плавлення: 560 °
Зовнішній вигляд: білий або брудно-білий порошок/кристалічна тверда речовина
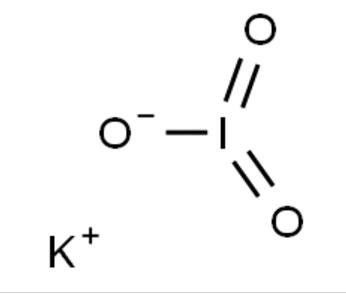
Йодат калію — це багата на йод сіль з формулою KIO3. У жаркому та вологому кліматі пари йоду гідролізуються через гігроскопічність йодиду калію. Порівняно з йодидом калію, йодат калію є більш стабільним і має довший термін зберігання. Він є потужним блокатором поглинання радіоактивного йоду щитовидною залозою.
Властивості продукту
Йодат калію — безбарвний моноклінний кристал або білий кристалічний порошок. Без запаху. Розчинний у воді, розведеній кислоті, водних розчинах етилендіаміну, етаноламіну та йодиду калію; мало розчинний у рідкому діоксиді сірки; нерозчинний у спиртах та аміаку.
Безбарвні кристали або білий порошок; моноклінічна структура; густина 3,90 г/см3; стабільний за звичайних температур; плавиться при 560°C з частковим розкладанням, виділяючи кисень; помірно розчинний у холодній воді; 4,74 г/100 мл при 0°C; більша розчинність у киплячій воді 32,3 г/100 мл при 100°C; розчинний у розчині йодиду калію; нерозчинний у спирті та рідкому аміаку.
Застосування
1) Йодат калію – це джерело йоду, яке отримують шляхом реакції йоду з гідроксидом калію. Це кристалічний порошок, стабільніший за йодид. Він має розчинність 1 г у 15 мл води. Використовується як швидкодіючий покращувач тіста; використовується з броматом калію як окислювачем для модифікації білка в хлібному борошні, що сприяє збільшенню об'єму та форми буханця. Використовується у випічці.
2) Йодат калію є досить сильним окислювачем, який може бути використаний для аналізу низки фармацевтичних речовин, наприклад: бензалконію хлориду, цетриміду, гідралазину гідрохлориду, калію йодиду, фенілгідразину гідрохлориду, семікарбазиду гідрохлориду тощо. За відповідних експериментальних параметрів йодат кількісно реагує як з йодидами, так і з йодом. Однак цікаво відзначити, що титрування йодатом може бути ефективно проведене в присутності насичених органічних кислот, спирту та багатьох інших органічних речовин.
Окисно-відновні методи з йодатом калію незмінно базуються на утворенні монохлориду йоду (ICl) у середовищі міцного розчину хлоридної кислоти.
3) Йод можна додавати до солі у формі йодиду калію (KI) або йодату калію (KIO3). Оскільки KIO3 має вищу стабільність у присутності домішок солі, вологості та пористої упаковки, це рекомендована форма.
Йодат калію, який утворюється як вторинний продукт, відновлюють активованим вугіллям. Продукт очищають кристалізацією з води. Як варіант, йодид заліза (II), отриманий з використанням порошку заліза та йоду, можна обробити карбонатом калію для отримання йодиду калію. Високочистий йодид калію можна отримати реакцією бікарбонату калію з йодистоводневою кислотою.
Інформація про транспорт
Номер ООН: 1479
Клас небезпеки: 5.1
Група упаковки: II
КОД ТН ЗЕСЬ: 28299080
Рекомендовані продукти
Специфікація
| Елемент аналізу | Стандартний | Результат аналізу |
| Опис | Білий або брудно-білий порошок/кристалічна тверда речовина | Відповідає |
| Втрати при сушінні% | ≤0,5% | 0,03% |
| I(%)≤ | 0,0019% | <0,002% |
| CLO3 (%) ≤ | 0,01% | <0,01% |
| SO4 (%) ≤ | Відповідає | Відповідає |
| Важкий метал (Pb)(%)≤ | <0,001% | <0,001% |
| PH | 5~8 | 6.0 |
| Як (%) ≤ | ≤0,0003% | <0,0003% |
| Аналіз | KIO3≥99,0% | 99,5% |








